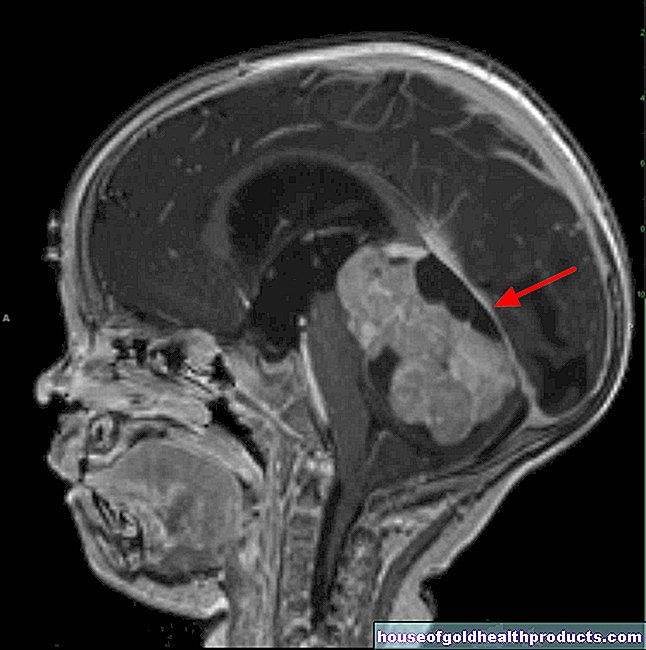
Müelofibroos
Astrid Leitner õppis Viinis veterinaariat. Pärast kümmet aastat veterinaarpraktikas ja tütre sündi läks ta juhuslikult üle meditsiiniajakirjandusele. Kiiresti selgus, et tema huvi meditsiiniteemade vastu ja armastus kirjutada on tema jaoks ideaalne kombinatsioon. Astrid Leitner elab koos tütre, koera ja kassiga Viinis ja Ülem -Austrias.
Lisateavei ekspertide kohta Kogui sisu kontrollivad meditsiiniajakirjanikud.Müelofibroos on krooniline luuüdihaigus, mis kuulub müeloproliferatiivsete neoplaasiate rühma. Aja jooksul kaotab inimeste luuüdi võime vererakke valmistada. Loe siit, kuidas haigus areneb, millised märgid viitavad müelofibroosile ja kuidas seda ravitakse!
Selle haiguse ICD -koodid: ICD -koodid on rahvusvaheliselt tunnustatud meditsiiniliste diagnooside koodid. Neid võib leida näiteks arsti kirjadest või töövõimetuslehtedelt. D47

Lühiülevaade
- Mis on müelofibroos? Müelofibroos on krooniline ja progresseeruv haigus, mille korral luuüdi muutub sidekoeks ja kaotab seeläbi vererakkude tootmise võime.
- Haiguse käik ja prognoos: Haiguse kulg on inimestel erinev. Haigust saab ravida ainult harvadel juhtudel, kuid sageli on see aeglane.
- Ravi: ravi on suunatud sümptomite leevendamisele ja elukvaliteedi parandamisele. Jälgimine ja ootamine (ootamine ja arstide regulaarne kontroll), ravimid (sihipärane ravi niinimetatud JAK2 inhibiitoritega), kiiritus või põrna eemaldamine, tüvirakkude siirdamine
- Põhjused: Müelofibroosi põhjustavad luuüdi vereloomerakkude geenimuutused. Kuidas see juhtub, on suuresti teadmata.
- Riskifaktorid: puuduvad riskifaktorid, mis muudavad haiguse tõenäolisemaks, kuid mõnedel inimestel on pärilik kalduvus müelofibroosi tekkeks.
- Sümptomid: väsimus, õhupuudus, südamepekslemine, kalduvus korduvatele infektsioonidele ja verehüüvetele, naha ja limaskestade verejooks, kehakaalu langus, ülakõhuvalu, peavalu, palavik, öine higistamine
- Diagnostika: vereanalüüsid (sageli juhuslikud tulemused!), Luuüdi biopsia, ultraheli ja põrna ja maksa kompuutertomograafia, molekulaarne geneetiline uuring
- Ennetamine: ennetavaid meetmeid pole võimalik rakendada
Mis on müelofibroos?
Müelofibroos on krooniline haigus, mille korral luuüdi muutub sidekoeks ja kaotab vererakkude tootmise võime. Mõiste on tuletatud kreeka sõnast myelós, mis tähendab luuüdi. Fibroos kirjeldab elundite sidekoe patoloogilist suurenemist.
Teised müelofibroosi nimetused on "osteomüelofibroos" (OMF), "krooniline müeloproliferatiivne haigus" (CMPE) ja "krooniline idiopaatiline müelofibroos" (CIMF). Need terminid on aga aegunud ja neid pole meditsiiniringkondades juba mitu aastat kasutatud.
Kuidas normaalne vereloome toimib?
Luuüdi on keha kõige olulisem vereloomeorgan. See koosneb sidekoest ja tüvirakkudest, mis muu hulgas toodavad vererakke. Seda leidub peamiselt pikkades luudes (nt õlavarre- ja reieluudes), selgroolülides ja vaagnaluudes. Funktsionaalsed vererakud küpsevad tüvirakkudest mitmel vaheetapil. Nende hulka kuuluvad punased ja valged verelibled ja trombotsüüdid. Arstid nimetavad vererakkude moodustumise protsessi vereloomeks.
Mis juhtub müelofibroosiga?
Müelofibroosi korral põhjustab tüvirakkude talitlushäire esialgu luuüdi ja vererakkude tootmise suurenemist. Pikemas perspektiivis asendatakse luuüdi järk -järgult sidekoega. Lõpuks kaotab see vererakkude tootmise võime.
Uute vererakkude tootmiseks kantakse vere moodustumine teistesse organitesse (põrn, maks). Arstid nimetavad seda ekstramedullaarseks (väljaspool luuüdi) vere moodustumiseks. Alguses on veel võimalik rahuldada vererakkude vajadust. Müelofibroosi hilisemates etappides ei suuda maks ja põrn enam piisavalt rakke toota - vererakkude moodustumine peatub.
Müelofibroosi vormid
Müelofibroos koos polütsüteemiaga (PV) ja essentsiaalse trombotsüteemiaga (ET) kuulub krooniliste müeloproliferatiivsete neoplaasiate (MPN) rühma. Nende ühine joon on see, et kõigi haiguste korral toodetakse luuüdis rohkem vererakke või sidekoerakke.
Müelofibroos esineb kahel kujul:
Primaarne müelofibroos (PMF): primaarne müelofibroos areneb elu jooksul juhuslikult, ilma eelneva haiguseta. See on müelofibroosi kõige levinum vorm.
Sekundaarne müelofibroos (SMF): sekundaarne müelofibroos areneb olemasolevast haigusest (PV või ET).
sagedus
Müelofibroos on üks haruldasi haigusi: igal aastal areneb see 0,5–1,5 100 000 inimese kohta. Haigus esineb valdavalt vanemas eas: keskmiselt on patsiendid diagnoosimise ajal 65 -aastased, mehed kannatavad mõnevõrra sagedamini kui naised 65 -protsendiliselt. Noored täiskasvanud on suhteliselt haruldased ja lastel PMF praktiliselt puudub.
Kas müelofibroos on surmav / ravitav?
muidugi
Müelofibroos on patsienditi väga erinev. Ei saa ennustada, millisel patsiendil haigus areneb aeglaselt ja millisel patsiendil kiiremini. Seetõttu ei saa eeldatava eluea kohta üldist avaldust teha. Kuigi mõned patsiendid elavad aastaid ilma sümptomiteta, progresseerub haigus teistel kiiresti ja lõpeb lõppkokkuvõttes surmavalt kuude või mõne aasta pärast. Kõige sagedasemad surmapõhjused on üleminek ägedale müeloidsele leukeemiale, südame -veresoonkonna haigused ja infektsioonid.
prognoos
Müelofibroosi prognoosi jaoks on määrav haiguse individuaalne käik. Nende hulka kuuluvad sellised tegurid nagu patsiendi vanus, sümptomid ja vere väärtused (vererakkude arv, hemoglobiini väärtus). Teine prognoosi mõjutav tegur on see, kas ja kui hästi patsient ravile reageerib.
Vaatamata kaasaegsetele ravimitele ja erinevatele ravivõimalustele saab müelofibroosi praegu ravida ravimitega ainult harvadel juhtudel ja ainult tüvirakkude siirdamisega. Umbes 20 protsendil kõigist haigestunutest muutub müelofibroos hoolimata ravist ägedaks leukeemiaks (verevähk).
Kuidas müelofibroosi ravitakse?
Müelofibroosi ravi on tavaliselt suunatud haiguse sümptomite leevendamisele ja elukvaliteedi säilitamisele. Hoolimata kaasaegsetest ravimeetoditest ei ole enamikul juhtudel võimalik ravimitega täielikult ravida. Ainus viis haigusest vabaneda on tüvirakkude siirdamine. Sellega kaasnevad aga riskid ja see ei sobi igale müelofibroosiga patsiendile.
Ravi haiguse varases staadiumis
Jälgige ja oodake: mitte iga patsient ei vaja kohe ravimteraapiat. Patsientidel, kellel pole sümptomeid, ootab arst tavaliselt ja viib läbi regulaarseid kontrolle. Patsient saab ravi alles esimeste sümptomite ilmnemisel. Kui patsient ja arst otsustavad strateegia "Vaata ja oota" kasuks, on oluline kinni pidada kokkulepitud kontrollkohtumistest (nt vereanalüüsid) ja pöörata tähelepanu tüüpilistele sümptomitele.
Uute vererakkude moodustumist pärssivad ravimid: Haiguse alguses toodab luuüdi esialgu suurt hulka vererakke. Selles faasis võib osutuda vajalikuks kasutada ravimeid, mis pärsivad uute vererakkude teket.
Ravi haiguse hilises staadiumis
Haiguse progresseerumisel tekib üha vähem vererakke, mis põhjustab aneemiat ja müelofibroosi tüüpilisi sümptomeid.
Vereülekanne: vereülekanne aitab hoida punaste vereliblede arvu stabiilsena ja leevendada aneemia sümptomeid (kahvatus, väsimus, hingamisraskused).
Janus kinaasi inhibiitorid (JAK2 inhibiitorid): Müelofibroosi raviks kasutatavad niinimetatud Janus kinaasi inhibiitorid on olnud turul juba paar aastat. Toimeaine ruksolitiniib on tavaliselt hästi talutav ja parandab paljudel juhtudel sümptomeid. Märkimisväärselt vähenevad sellised sümptomid nagu palavik, öine higistamine, luuvalu ja kehakaalu langus. Samuti vähendavad nad põrna ja maksa suurust. Ravi kestus ei ole ajaliselt piiratud.
Interferoonid: Sarnased tulemused nagu JAK2 inhibiitorite puhul (põrna suuruse vähenemine) saavutatakse nn interferoonidega. Neid kasutatakse peamiselt müelofibroosi väga varases vormis.
Kortisoon: Kortisooni preparaate kasutatakse eriti patsientidel, kellel tekib palavik. Mõnel juhul parandavad nad aneemiat, kuid on vastuolulised, kuna pärsivad samal ajal immuunsüsteemi.
Põrna kiirgus: kiirgus vähendab põrna suurust ja leevendab seega seedetrakti kaebusi. Kuid nende suurus kasvab aja jooksul tagasi ja ravi tuleb võib -olla korrata.
Põrna eemaldamine (splenektoomia): Müelofibroosi hilises faasis on põrn tavaliselt oluliselt laienenud. See avaldab survet maole ja soolestikule, põhjustades valu ja seedehäireid (kõhulahtisus, kõhukinnisus). Põrna eemaldamist seostatakse veresoonte oklusiooni (tromboosi) suurenenud riskiga: muu hulgas on põrn vereliistakute hoiukohana. Kui see eemaldatakse, suureneb trombotsüütide arv veres. See suurendab verehüüvete tekke riski.
Tüvirakkude siirdamine: Ainus viis müelofibroosi ravimiseks on praegu niinimetatud allogeenne tüvirakkude siirdamine. Selle protsessi käigus kantakse patsiendile üle terved tüvirakud doonori luuüdist või verest. “Allogeen” tähendab, et tüvirakud ei pärine patsiendilt endalt, vaid tervelt doonorilt. Ravi eesmärk on, et ülekantud vere tüvirakud moodustaksid taas iseenesest toimivad vererakud.
Et siirdatud luuüdi tagasi ei lükataks, saab patsient enne siirdamist nn konditsioneerimisravi. See lülitab välja keha enda kaitserakud, mis suurendab oluliselt patsiendi vastuvõtlikkust infektsioonidele. Kuni siirdatud luuüdi hakkab toimima ja toodab piisavalt vererakke, on patsient nakatumisoht oluliselt suurenenud.
Seetõttu on allogeenne tüvirakkude ravi vaid väikese grupi patsientide jaoks. Tavaliselt tehakse seda ainult noorematele patsientidele, kellel on raske müelofibroos, kuid muidu on nad heas seisukorras.
Dieet müelofibroosi korral
Müelofibroosi jaoks ei ole konkreetset soovitatud dieeti. Enamikul müelofibroosiga patsientidel tekivad maksa ja põrna suurenemise tõttu seedetrakti kaebused, nagu kõhukinnisus ja kõhupuhitus. Sellistel juhtudel on soovitatav tarbida piisavalt kiudaineid (teraviljad, puuviljad, köögiviljad), juua piisavalt ja vältida kõhupuhituslikke toite, nagu kapsas, köögiviljad ja sibul.
Millised on müelofibroosi sümptomid?
Müelofibroosi sümptomid sõltuvad haiguse staadiumist. Eriti haiguse alguses on sümptomid endiselt väga spetsiifilised. Sümptomid, nagu väsimus, kurnatus ja suurenenud vastuvõtlikkus infektsioonidele, esinevad ka paljude teiste haiguste taustal ega anna esialgu kahtlust haruldasele luuüdihaigusele. Sel põhjusel tehakse diagnoos tavaliselt hilja, kui vereanalüüs muutub -
sageli juhuslikult osana ennetavast arstlikust kontrollist.
Alles edasisel kursil tugevneb haigustunne. Tüüpilised sümptomid, mis tekivad müelofibroosi progresseerumisel, on järgmised:
- Valu ülakõhus ja enneaegne puhitus, mis on tingitud põrna ja maksa suurenemisest
- Seedehäired nagu kõhulahtisus, kõhukinnisus
- kõrvetised
- Väike isu, kaalulangus
- Emboolia ja tromboos
- kahvatus
- Õhupuudus
- Öine higistamine
- palavik
- Torkimistunne ja halb vereringe kätes ja jalgades
- Sügelus (eriti PV)
- Luu- ja liigesevalu (haiguse hilisemas staadiumis)
- Suurenenud kalduvus veritseda (sageli verevalumid, ninaverejooks)
Põhjused ja riskitegurid
Müelofibroosi täpsed põhjused pole teada. Umbes 65 protsendil kõigist müelofibroosiga patsientidest leiavad arstid patsientide vere tüvirakkudes kromosoomi 9 iseloomuliku geenimuutuse. Seda geneetilist muutust, mida tuntakse JAK2 mutatsioonina (Januskinase2 mutatsioon), leidub ka mõnedel polütsüteemia veraga patsientidel ( PV) ja tuvastatavat essentsiaalset trombotsüteemiat (ET).
JAK2 mutatsioon põhjustab valgete vereliblede ja trombotsüütide paljunemist kontrollimatul viisil. Vererakkude massiline moodustumine stimuleerib samaaegselt nn "kasvufaktorite" teket. Need omakorda stimuleerivad luuüdi rakke sidekoe rakkude tootmiseks. Luuüdi nihutab üha enam sidekoe, mistõttu moodustuvad üha vähem funktsionaalsed vererakud. Keha püüab puudust kompenseerida ja suunab veretootmise teistesse elunditesse. Vererakke toodetakse praegu peamiselt põrnas ja vähemal määral maksas. Tulemus: mõlemad elundid suurenevad. Kuidas käivitav geneetiline muutus toimub, pole teada.
Riskifaktorid
Vanus on primaarse müelofibroosi tekkimise suurim riskitegur. Mida kõrgem on vanus, seda suurem on JAK2 mutatsiooni tõenäosus. Praegu puuduvad tõendid selle kohta, et teatud elustiil või välismõjud, näiteks ioniseeriv kiirgus või keemilised ained suurendavad haigestumise tõenäosust.
Sekundaarne müelofibroos areneb teistest kroonilistest müeloproliferatiivsetest haigustest. Polütsüteemia vera või essentsiaalse trombotsüteemia diagnoos suurendab müelofibroosi tekkimise riski.
Kas müelofibroos on pärilik?
Paljudel juhtudel käivitab müelofibroosi vere moodustavate tüvirakkude geneetiline muutus. Tavaliselt areneb mutatsioon elu jooksul spontaanselt ja seda ei edastata. Kuidas see juhtub, pole veel selgitatud.
Kuid kroonilised müeloproliferatiivsed haigused on mõnes peres tavalisemad. Arstid eeldavad, et haigestunutel on nende haiguste suhtes pärilik kalduvus: neil on geneetiline materjal, mis soodustab mutatsiooni (JAK2 mutatsioon) tekkimist. Kuid ainult ühel protsendil sellise tendentsiga inimestest tekib tegelikult müelofibroos.
Uurimine ja diagnoosimine
Ligikaudu veerandil patsientidest ei ole müelofibroosi diagnoosimisel mingeid sümptomeid. Kuna sümptomid on väga spetsiifilised, eriti haiguse alguses (väsimus, väsimus, suurenenud vastuvõtlikkus infektsioonidele), siis enamik müelofibroosiga patsiente pöördub arsti poole alles hilja. Muutunud vereväärtusi märkab perearst tavaliselt muude uuringute käigus (nt ennetav tervisekontroll). Kui kahtlustatakse kroonilist müeloproliferatiivset haigust, suunab perearst patsiendi tavaliselt hematoloogi (verehaiguste spetsialist) juurde.
Füüsiline läbivaatus: füüsilise läbivaatuse käigus palpeerib arst muu hulgas kõhtu, et teha kindlaks, kas põrn ja / või maks on suurenenud.
Vereanalüüs: haiguse alguses on ülekaalus vereliistakute ja mõõdukas valgete vereliblede arv. Hiljem muutub rakkude jaotus vereanalüüsis - tekib punaste ja valgete vereliblede ning trombotsüütide puudus. Samuti on punaste vereliblede kuju tavaliselt muutunud. Need ei ole enam ümarad, vaid on "pisarakujulised".
Ultraheliuuring: ultraheliuuring võib määrata põrna ja maksa suurenemise.
Molekulaarne geneetiline testimine: umbes 65 protsendil kõigist müelofibroosiga patsientidest on JAK2 mutatsioon. Seda saab tuvastada spetsiaalse vereanalüüsi abil.
Luuüdi aspiratsioon: Kuna JAK2 mutatsioone esineb ka teiste haiguste, näiteks PV ja ET korral, on järgmine samm luuüdi aspiratsioon. Tüüpiliste muutuste põhjal saab müelofibroosi usaldusväärselt diagnoosida. Selleks võtab arst kohaliku anesteesia all vaagnaluu luuüdist proove ja uurib neid mikroskoobi all tüüpiliste muutuste suhtes.
Reeglina võetakse luust kaks erinevat proovi: ühelt poolt imetakse vedel luuüdi õhukese nõelaga ära ja teiselt poolt teeb arst stantsbiopsia. Selleks eemaldab ta vaagnaluust väikese luusilindri. Haiguse lõppfaasis juhtub, et enam pole vedelat luuüdi. Seejärel räägivad arstid "kuivast luuüdist".
Ennetada
Kuna müelofibroosi täpne põhjus pole teada, ei ole haiguse ennetamiseks teaduslikke soovitusi. Kui müelofibroos või muud kroonilised müeloproliferatiivsed haigused (ET, PV) esinevad peredes ja vähemalt kolme põlvkonna jooksul, soovitavad arstid geneetilist nõustamist. Seejärel hindab inimese geneetika spetsialist riski, et haigus ilmneb kavandatud järglastel, eriti kui nad soovivad lapsi saada.
Sildid: hambaravi intervjuu digitaalne tervis